原电池的工作原理
以下为《原电池的工作原理》的无排版文字预览,完整格式请下载
下载前请仔细阅读文字预览以及下方图片预览。图片预览是什么样的,下载的文档就是什么样的。
原电池的工作原理
**_*学
牛某某教学重点: 1、原电池的构造特点及工作原理。
2、原电池电极及电池反应式的书写。
3、简单原电池的设计。
教学难点:1、电极反应式的书写。
2、简单的原电池设计。判断下列装置能否构成原电池,并思考原电池的构成条件 ZnCu知识回顾1.总结:构成原电池的条件(1)有自发进行的氧化还原反应(前提) (2)有两个活泼性不同的电极
(不同的金属或金属与非金属导体)作电极(3)两个电极必须插入电解质溶液中 (4)两极相连形成闭合回路 (用导线连接或电
极直接接触)还原剂(Zn)失去电子,发生氧化反应氧化剂(H+)在铜极上得到电子,发生还原反应还原剂失去的电子从锌极流出流入铜极经外电路Zn2+H+SO42-电流方向2.Cu-Zn稀硫酸原电池的工作原理:原电池中正极的判断方法: 归纳总结1.根据电极材料来判断:一般较不活泼的金属或非金属
(如石墨)作正极
2.根据电极反应来判断:发生还原反应的一极是正极3.根据电子(或电流)的流向来判断:电子流入(或电流流出)的一极是正极4.根据电解质溶液中离子的移动方向来判断:阳离子移向的一极是正极5.根据电极现象来判断:质量增重或有气泡产生的一极是正极
【思考】左图的装置能否构成原电池?如果不能,请说明理由;如果能,标出正负极。C下列哪些装置能构成原电池?标出正负极,写出相应的电极反应式。交流讨论一Zn负极Zn: Zn-2e- =Zn2+正极C:2H++2e- =H2↑总反应:Zn+2H+=Zn2++H2↑负极Cu: Cu-2e- =Cu2+正极C:2Ag++2e- =2Ag总反应:Cu+2Ag+=Cu2++2Ag【拓展引申】一种新型燃料电池,它是以两根金属铂片插入
KOH溶液中作电极,又在两极上分别通入甲烷
和氧气。电极反应为:
负极:
正极:
电池总反应:
2O2+ 4H2O +8e-= 8OH -CH4+ 10OH --8e-= CO32- + 7H2OCH4+ 2O2 + 2KOH = K2CO3 + 3 H2O【思考】将上述原电池的电解质溶液换成H2SO4溶液,那么
负极:
正极:
电池总反应: CH4 -- 8e- + 2H2O == 8H+ + CO2 2O2 + 8e- + 8H+ == 4H2O? CH4 + 2O2 === CO2 + 2H2O【总结】电极反应式书写书写方法:
1、先确定原电池的正负极,列出正负极上的反 应物质。
2、考虑电解质溶液参与反应。
3、正负极反应式相加得到电池反应的总反应式。注意事项:
1.两极得失电子数目相等
2.电极反应式常用“=”不用“→”
3.有气体生成需加“↑”
【过渡】给出一个原电池的装置图,我们能够判断出正负极并可写出相应的电极反应式和总反应,那么,我们可不可以结合学过的知识,将一个具体的氧化还原反应设计成原电池呢?交流讨论二1.利用反应Cu + 2FeCl3 = 2FeCl2 + CuCl2,
设计一个单池原电池,画出原电池的装置图,标出电极材料,电解质溶液,写出电极反应。 参考答案 (-)负极(Cu): Cu-2e-=Cu2+(氧化反应)
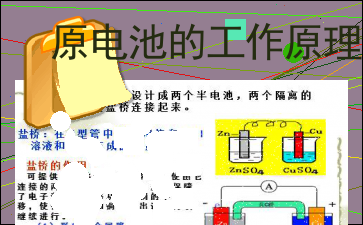
正极(Pt或C):2Fe3++2e-=2Fe2+(还原反应)【思考】单池原电池效率低,并且一段时间后,电流会减弱,那么我们如何获得持续稳定的电流呢?友情提示可将单池原电池设计成两个半电池,两个隔离的半电池通过盐桥连接起来。盐桥:在U型管中装满用饱和KCl溶液和琼脂作成的冻胶。盐桥的作用:
可提供定向移动的阴阳离子,使由它连接的两溶液保持电中性,盐桥保障了电子通过外电路从锌到铜的不断转移,使锌的溶解和铜的析出过程得以继续进行。
(1)形成闭合回路
(2)平衡电荷交流讨论三利用反应Cu + 2FeCl3 = 2FeCl2 + CuCl2,
设计一个双池原电池,使其能获得持续稳定的电流。画出原电池的装置图,标出电极材料,电解质溶液,写出电极反应,并与之前设计的单电池对比找出他们有什么共 同点。 参考答案 (-)负极(Cu): Cu-2e-=Cu2+(氧化反应)
正极(Pt或C):2Fe3++2e-=2Fe2+(还原反应)(-)(+)单池与双池的反应实质相同根据氧化还原反应设计原电池:1.改:将化学反应方程式改写成离子方程式
2.拆:根据反应前后的价态变化将氧化反应和还原反应拆开书写(即电极反应)
3.定:根据电极反应确定电极材料
4.画:画出原电池的装置图【总结】
当堂检测1、判断下列哪些装置构成了原电池?若不是,请说明理由;若是,请指出正负极名称,并写出电极反应式.
( X )负极:Zn-2e-=Zn2+2H++2e-=H2↑正极:总反应:Zn+2H+=Zn2++H2↑看看谁学会了2、判断正误:
(1).在原电池中,发生还原反应的一极为原电池的负极。( )
(2).在原电池中不断溶解的一极为原电池的正极。( )
(3).在Cu-Zn稀硫酸原电池中,SO42-向正极移动。( )
(4).电流由原电池的负极流向正极。( )
(5).原电池的两极,一定是由活动性不同的两种金属组成( )
(6).电子从发生还原反应的电极流出。( )××××××3、一个原电池的总反应的离子方程式是Zn + Cu2+ =
Zn2+ + Cu,该反应的原电池的组成正确的是
C4.依据氧化还原反应:2Ag+(aq)+Cu(s) = Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:
(1)电极X的材料是________;
电解质溶液Y是___________;
(2)银电极为原电池的________极,发生的电极反应_________________;X电极上发生的电极反应为____________________________;
外电路中的电子是从_______极流向________电极。CuAgNO3溶液正2Ag++2e-=2AgCu-2e-=Cu2+CuAg4.原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关。下列说法不正确的是( ) A.由Al、Cu、稀H2SO4组成的原电池,其负极反应式为:
Al-3e-=Al3+
B.由Mg、Al、NaOH溶液组成的原电池,其负极反应式为:
Al-3e-+4OH-=AlO2-+2H2O
C.由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为:
Cu-2e-=Cu2+
D.由Al、Cu、浓硝酸组成原电池,其负极反应式为:
Cu-2e-=Cu2+ C【学以致用】日常生活中,我们所使用的铁制品很容易生锈,请你用学过的原电池的知识,分析其生锈的原因。试写出电极材料、电极反应方程式及总反应。
1.通过本堂课的学习,理解原电池的工作原理
2.会设计简单的原电池并能正确书写电极反应方程式 课堂总结
[全文已结束,注意以上仅为全文的文字预览,不包含图片和表格以及排版]
以上为《原电池的工作原理》的无排版文字预览,完整格式请下载
下载前请仔细阅读上面文字预览以及下方图片预览。图片预览是什么样的,下载的文档就是什么样的。
图片预览