原电池修改
以下为《原电池修改》的无排版文字预览,完整格式请下载
下载前请仔细阅读文字预览以及下方图片预览。图片预览是什么样的,下载的文档就是什么样的。
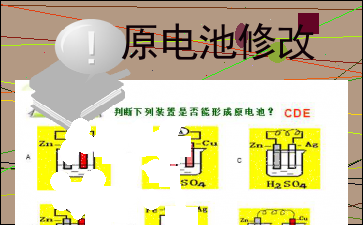
1、体验化学能与电能相互转化的探究过程,了 解原电池和电解池的工作原理,能写出电极反应和电池反应方程式。 2、了解常见化学电源的种类及其工作原理,认识化学能与电能相互转化的实际意义及其重要应用。 ?3、能解释金属发生电化学腐蚀的原因,认识金属腐蚀的危害,通过实验探究防止金属腐蚀的措施。 电化学课标要求 化学能与电能的转化 原电池的工作原理一、原电池1、定义:化学能转化为电能的装置。练习判断下列装置是否能形成原电池?ABCDEFCDE2、原电池的形成条件 形成闭合回路
两电极用导线连接或接触。能自发进行的氧化还原反应 电解质溶液
溶液中存在自由移动的阴阳离子,能导电。 两导体作电极
①活动性不同的金属(或一种金属和一种非金属导
体石墨),活泼金属为负极。
②两惰性电极——石墨或Pt等(燃料电池电极)。发生原电池的反应通常是放热反应,在理论上可设计成原电池的化学反应是 ( )
A. C(s)+H2O(g)=CO(g)+H2(g); △H>0
B. Ba(OH)2·8H2O(s)+2NH4Cl(s)
=BaCl2(1)+2NH3·H2O(1)+8H2O(1);△H>0
C. CaC2(s)+2H2O(1)→Ca(OH)2(s)+C2H2(g);
△HB。(3)设计原电池。(5)制作化学电源。(4)用于金属的防护。(被保护金属作正极) 三、原电池正、负极的判断方法:(1)根据组成原电池两极的材料判断:一般活泼金属为负极。
活泼性较弱的金属或石墨为正极。(2)根据现象判断:一般溶解的一极为负极;
增重或有气泡放出的一极为正极。(3)根据两极的反应判断:发生氧化反应的为负极;
发生还原反应的为正极。(4)根据电流方向或电子流动方向判断:电子流出的为负极。
电子流入的为正极(5)根据电解质溶液内离子的定向移动判断:溶液中阳离子移向正极;
阴离子移向负极。特别提醒:
1.Mg、Al、NaOH溶液构成的原电池,
Al为负极;Cu为负极。2.Fe(或Al)、Cu、浓硝酸构成的原电池,生活中我们常使用各种各样的电池用于“神七”的太阳能电池笔记本电脑专用电池手机专用电池一、电池的种类及特点一次电池:二次电池:燃料电池:活性物质发生氧化还原反应被消耗到一定程度后,就不能再使用可反复充电和放电能量利用率高,可连续使用,污染轻如锌锰干电池、银锌钮扣电池等如铅蓄电池、锂电池等如氢氧燃料电池二、常见电池1.一次电池银锌钮扣电池正极:负极:电解质溶液:H2O+Ag2O+Zn===2Ag+Zn(OH)2电池反应:ZnAg2OKOH溶液Zn+2OH--2e-===Zn(OH)2负极:H2O+Ag2O+2e-===2Ag+2OH-正极:碱性锌锰电池
正极:负极:电解质:电池反应:Zn金属棒KOH正极:Zn+2MnO2+2H2O===Zn(OH)2+2MnOOH2MnO2+2H2O+2e-===2MnOOH+2OH-Zn+2OH--2e-===Zn(OH)2负极:2.氢氧燃料电池:总反应为:2H2+O2==2H2O(1)电解质溶液为KOH溶液2H2 + 4OH- - 4e- = 4H2OO2 + 2H2O + 4e- = 4OH-正极:负极:(2)电解质溶液为H2SO4溶液正极:负极:O2 +4H+ + 4e- =2H2OH2-2e- = 2H+(3)固体电解质正极:O2 + 4e- = 2O2-2H2 + 2O2- - 4e- = 2H2O负极:(4)熔融碳酸盐(如:熔融K2CO3)正极:O2 +2CO2+ 4e- = 2CO32-H2 + CO32- - 2e- = H2O+CO2负极:思考1:如把H2改为CH4,KOH溶液作电解液,形成燃料电池,
总反应式:
电极反应: 负极
正极
CH4 -8e- +10 OH- = CO32-+7H2OO2 +4e- +2H2O =4OH-CH4+2OH-+2O2= CO32 -+3H2O思考2:如把CH4改为甲醇(CH3OH),KOH溶液作电解液,形成
燃料电池,你能写出其正负极的电极反应式吗? 负极:正极:O2 +4e- +2H2O =4OH-2CH3OH + 4OH- + 3O2= 2CO32 -+ 6H2O电池反应:(1)电极材料及原料
(2)电解质溶液
正极:PbO2 负极:PbH2SO4溶液负极(Pb): Pb- 2e-+ SO4 2 - =PbSO4正极(PbO2): PbO2+4H++SO42 -+ 2e-= PbSO4 +2H2O总反应:3.二次电池铅蓄电池(3)放电时电极反应式:(4)充电时电极反应式:阴极:阳极:由铅蓄电池的总反应可知,随着放电反应的进行,硫酸的浓度
不断下降,密度不断减小,人们常根据硫酸密度大小来判断
铅蓄电池是否需要充电充电过程总反应:2PbSO4+2H2O=Pb+PbO2+2H2SO4
蓄电池在放电时起原电池的作用,在充电时起电解池的作用。下面是爱迪生蓄电池分别在充电和放电时发生的反应:
Fe+NiO2+2H2O Fe(OH)2+Ni(OH)2
下列有关爱迪生蓄电池的推断错误的是 ( )
A.放电时,Fe是负极,NiO2是正极
B.蓄电池的电极可以浸入某种酸性电解质溶液中
C.充电时,阴极上的电极反应为:Fe(OH)2+2e-=Fe+2OH-
D.放电时,电解质溶液中的阴离子向正极方向移动BD
[全文已结束,注意以上仅为全文的文字预览,不包含图片和表格以及排版]
以上为《原电池修改》的无排版文字预览,完整格式请下载
下载前请仔细阅读上面文字预览以及下方图片预览。图片预览是什么样的,下载的文档就是什么样的。
图片预览